Wie gefährlich sind therapeutische Nanopartikel?
Kleinste Teilchen sollen Wirkstoffe gezielt in den Körper transportieren oder Gewebe erwärmen. Kurzfristig sind sie stabil und fügen Zellen keinen Schaden zu. Über langfristige Effekte können Forscher derzeit noch nichts sagen.
Bei schweren Erkrankungen wie Krebs versuchen Mediziner, Arzneistoffe in Nanopartikel zu verpacken. Erst vor Ort, etwa an einem Tumor, sollen die Pharmaka dann freigesetzt werden. Damit könnte man, so die Hoffnung, lokal hohe Konzentrationen erzielen, ohne dass es zu starken Nebenwirkungen kommt. Als Materialien für kleinste Teilchen sind Kohlenstoff oder Eisen im Gespräch, wobei das Metall rein physikalisch wirkt.
Doch wie verhalten sich diese Partikel im Organismus? Geht von ihnen selbst eine Gefahr aus? Damit haben sich Wissenschaftler der Heinrich-Heine-Universität Düsseldorf jetzt befasst. Sie wollten auch wissen, über welche Mechanismen unser Körper kleinste Teilchen entsorgt. Ihre Arbeiten beschäftigten sich speziell mit Kohlenstoff.
Kohlenstoff-Nanopartikel in der Zelle
Bei dem neuen Behandlungskonzept gehen erwünschte Eigenschaften mit potenziellen Gefahren einher. Aufgrund ihrer geringen Ausmaße, die Teilchen sind kleiner als fünf Nanometer, gelangen sie durch Barrieren im Körper. Schleimhäute stellen kein nennenswertes Hindernis dar. Und auch die Blut-Hirn-Schranke, eine Barriere zwischen dem Gehirn und dem restlichen Organismus, wird passiert. Das führt schon zum ersten Problem: Nanopartikel verteilen sich stark im Körper. Um sie beispielsweise an den Tumor zu bringen, braucht es spezifische Bindungsstellen auf der Oberfläche von Krebszellen und passende Gegenstücke auf den kleinsten Teilchen.
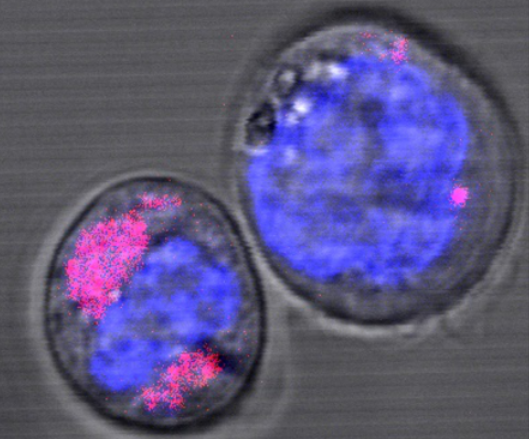
Im besten Fall gelangen Nanopartikel in ihre Zielstruktur und setzen dort einen Arzneistoff frei. Das Teilchen selbst bleibt in der Zelle. Forscher aus Düsseldorf haben diesen Teilschritt über Graphen-Nanopartikel simuliert. Die Teilchen bestehen aus zweidimensionalen Lagen von Kohlenstoff-Sechseckringen – und wurden in Stammzellen des blutbildenden Systems gebracht. Diese gelten als besonders empfindlich. Sie müssen ein Leben lang für neue Blutzellen sorgen. Mögliche Effekte seien weitaus stärker als bei robusteren Zellen, schreiben die Forscher.
Teilchen werden eingekapselt und entsorgt
Zu den Ergebnissen: Kohlenstoff-Nanopartikel gelangten wie gewünscht in die Zellen, wurden danach aber in speziellen Strukturen eingekapselt, den Lysosomen. Diese Organellen, sprich Strukturen innerhalb der Zelle, werden von einer Biomembran umschlossen. In ihrem Inneren befinden sich bei einem sauren pH-Wert verschiedene Verdauungsenzyme. Einen Abbauprozess beobachteten die Forscher allerdings über die Dauer ihrer Experimente – einige Tage – nicht. Damit bleibt unklar, was mit Kohlenstoff-Nanopartikeln weiter passiert. Geht eine Zelle als Ganzes zugrunde, kommen Fresszellen, die Makrophagen, ins Spiel. Sie könnten Reste aufnehmen und eliminieren, was hier jedoch nicht untersucht worden ist.
Dennoch haben die Düsseldorfer Experten eine gute Nachricht: Kleinste Teilchen beeinflussten die Aktivität von Genen nur unwesentlich. Verglichen sie Stammzellen mit und ohne Nanopartikel, gab es nur bei einem von insgesamt 20’800 untersuchten Ablesevorgängen im Erbgut deutliche Änderungen. Bei 1’171 weiteren Vorgängen wurden leichte Effekte gefunden.
„Die Einkapslung der Nanopartikel in den Lysosomen sorgt dafür, dass diese Teilchen zumindest für einige Tage – solange unsere Untersuchungen dauerten – sicher verwahrt sind und die Zelle nicht schädigen können“, fasst Thomas Heinzel zusammen. Er hat eine Professur am Institut für Experimentelle Festkörperphysik der Universität Düsseldorf. „Damit ist die Lebensfähigkeit der Zelle ohne wesentliche Änderung der Genexpression erhalten.“ Langzeitaussagen, die etwa eine erhöhte Wahrscheinlichkeit für eine Entartung der Zellen in Richtung Krebsentstehungen feststellen können, seien mit dem Experiment aber nicht möglich.
Eine Frage des Materials
Heinzel und seine Kollegen befassten sich mit Kohlenstoff. Schon länger sind bei Gehirntumoren jedoch Eisenoxid-Partikel im Gespräch. Sie werden als Suspension gespritzt, gelangen durch die Blut-Hirn-Schranke und reichern sich im Krebsgewebe an. Das gelingt aufgrund spezieller Beschichtungen auf der Oberfläche. Legen Ärzte ein magnetisches Wechselfeld an, erwärmen sich die kleinen Teilchen stark. Hitze soll die Geschwulst dabei zerstören oder empfindlicher gegenüber Chemotherapien machen.
Dabei stellt Eisenoxid kein Problem dar. Es ist in der eingesetzten Menge nicht toxisch und wird vom Körper abgebaut. Beispielsweise enthalten rote Blutkörperchen grosse Eisenmengen. Ärzte machen sich über Langzeiteffekte keine Gedanken, da Gehirntumoren je nach genauem Typ als extrem aggressiv gelten. Überleben Patienten einige Monate mehr, ist bereits viel gewonnen.
Quelle: https://www.ingenieur.de/technik/fachbereiche/nanotechnologie/wie-gefaehrlich-sind-therapeutische-nanopartikel/
Originalartikel und Bildquelle: "The low Toxicity of Graphene Quantum Dots is Reflected by Marginal Gene Expression Changes of Primary Human Hematopoietic Stem Cells"